2023-11-28
创新之路︱精挑细琢!深度揭秘阿得贝利单抗的改造全过程
编者按
医药创新,造福患者。但很多人也许不知道,一款创新药从研发到上市,往往要十年甚至数十年的漫漫求索路。恒瑞医药微信公众号推出《创新之路》栏目,我们希望通过讲述国产创新药诞生背后的故事,展现中国科研工作者担当和作为,营造创新发展良好氛围,并为我国医药创新实践提供一份思考的力量。
11月是“国际肺癌关注月”,让我们一起揭秘中国首个获批小细胞肺癌适应症的自主研发PD-L1抑制剂背后的研发故事。今年3月,中国首个获批小细胞肺癌适应症的自主研发PD-L1抑制剂、恒瑞医药1类新药阿得贝利单抗(艾瑞利®)获批上市,打破了3年来进口PD-L1抑制剂产品在治疗广泛期小细胞肺癌(ES-SCLC)领域的垄断地位,为中国小细胞肺癌患者带去治疗新希望。阿得贝利单抗守护患者生命健康背后,是一条怎样的自主研发之路?医疗媒体《奇点网》对阿得贝利单抗的研发历程进行报道,我们特别转载了这篇文章,分享给大家。
前言
在全球范围内,肺癌是发生率第二高的癌症,也是癌症死亡的主要原因。
小细胞肺癌(SCLC)约占所有肺癌的15%,它进展迅速,而且在早期就发生转移。据统计,大约70%的患者确诊时就已经处于广泛期[1]。
科学家为了开发新疗法做出了巨大努力,然而几十年来以铂类为基础的化疗仍然是广泛期SCLC(ES-SCLC)的标准一线治疗方案,这些治疗方案的中位总生存期为9-11个月[2]。
PD-L1抑制剂的出现,改变了ES-SCLC的治疗框架。在IMpower133[3,4]和CASPIAN[5,6]研究中,与化疗相比,PD-L1抑制剂联合化疗给ES-SCLC患者带来了总生存期的显著改善。由吉林省肿瘤医院程颖教授和中国医学科学院肿瘤医院王洁教授共同担任主要研究者的CAPSTONE-1研究,又将PD-L1抑制剂联合化疗治疗ES-SCLC的疗效提升到了新高度,该研究成果已发表在顶级医学期刊《柳叶刀·肿瘤学》杂志上。

▲ 论文首页截图
CAPSTONE-1研究数据表明,PD-L1抑制剂阿得贝利单抗联合化疗组的中位总生存时间(OS)达到了15.3个月,患者的死亡风险下降了28%(p=0.0017)。这也是迄今为止,PD-L1抑制剂联合化疗取得的最长中位OS(mOS)[7]。
阿得贝利单抗的优异表现,与恒瑞研发团队的精心设计密不可分。
精挑细琢,追求纯净
单克隆抗体已经成为治疗各类恶性肿瘤的重要手段。
与小分子药物不同,单克隆抗体药物除了可以阻断信号通路之外,还可以通过Fc段与效应免疫细胞表面的受体FcγR结合,介导免疫应答反应。这也是单克隆抗体发挥疗效的重要生物学基础。
例如,单克隆抗体的Fc段与FcγRI结合,可诱发抗体依赖性细胞因子释放(ADCR),Fc段与FcγRIIa结合可以介导抗体依赖性细胞介导的吞噬作用(ADCP),Fc段与FcγRIIIa结合可介导抗体依赖的细胞介导的细胞毒性作用(ADCC)[8-10]。此外,一些治疗性单克隆抗体还可以介导补体(C1q)依赖的细胞毒性作用(CDC)。简单来说,这些作用都会导致靶细胞死亡。
既往已上市的PD-L1抑制剂在抗体筛选时,考虑PD-L1表达在肿瘤细胞表面,除了阻断PD-L1/PD-1通路,恢复T细胞识别杀伤肿瘤的作用,同时会保留抗体Fc段与FcγR结合的能力,从而利用抗体Fc段的效应功能进一步杀伤肿瘤细胞。
然而,早在2015年就有文献报道,PD-L1不仅在肿瘤细胞表达,在包括T细胞、B细胞、巨噬细胞和树突状细胞(DCs)等免疫细胞上也有表达[11]。有文献指出,免疫检查点抑制剂,不希望免疫细胞耗尽,消除Fc段功能尤为重要[12]。
因此,恒瑞的研发团队在立项之初就确定,新开发的单克隆抗体只作为PD-1/PD-L1信号通路的抑制剂,尽可能消除对免疫细胞的潜在不良影响。这和之前进口药物的研发思路完全不一样。在这个大原则的指引下,天然没有CDC作用,且ADCC和ADCP作用较弱的lgG4型抗体成了首选。
基于设定的高亲和力、高阻断活性及高体外免疫刺激活性目标,恒瑞的研发团队从大量的杂交瘤抗体中筛选获得目标IgG4型抗体,并完成人源化。
在筛选到合适的靶向PD-L1的lgG4型抗体之后,接下来要做的就是进一步消除/降低ADCC、ADCP和ADCR作用。ADCR效应的降低,一方面可以减少IL-8的释放,增强免疫疗效,另一方面可以减少IL-6的释放,减少免疫相关不良反应的发生。
因此,恒瑞的研发团队给阿得贝利单抗的Fc段实施了234A/235A定点改造。改造后,与野生型IgG4型抗体相比,阿得贝利单抗与FcγRIIIa、FcγRIIa和FcγRI的亲和力显著降低。
以上的选择和改造,最大限度地降低了阿得贝利单抗的效应功能,对表达PD-L1的免疫细胞起到了很好的保护作用。从目前查阅的文献来看,阿得贝利单抗也是截至目前唯一一个公布Fc段改造位点的国产免疫检查点抑制剂。
不过,阿得贝利单抗的改造没有就此结束。由于在自然情况下,IgG4型抗体之间的抗原结合片段(Fab)会发生置换,形成一个新的双特异性抗体[13],而且这种置换还会导致不良反应的发生[14]。因此,研究人员得解决IgG4型抗体的这一弊病。
好在科学家早就找到了解决方案,只要给抗体Fab段实施S228P突变改造,就可以避免lgG4型抗体的Fab段置换,使抗体更稳定[13]。阿得贝利单抗的Fab段就采用了S228P突变改造。
与同类对比药物相比:阿得贝利单抗与PD-L1的结合角度更居中;结合区域更接近其天然受体PD-1;结合面积更接近其天然受体PD-1。
此外,衡量免疫检查点抑制剂的另外一个重要指标就是亲和力,即PD-1/PD-L1抑制剂与受体之间的结合力。亲和力的强弱,直接影响到了药物效果、临床的最佳剂量和部分不良反应程度。
亲和力常见评估指标为解离常数Kd,Kd表示处于平衡状态时配体与受体的解离程度,Kd值越大,说明解离越多,代表配体与受体之间的亲和力越弱;Kd值越小,说明解离越少,代表配体与受体间的亲和力越强。
研究数据显示,阿得贝利单抗的解离常数Kd值仅为0.27×10-10nmol/L较低,亲和力相较于已上市的PD-L1抑制剂更强[7]。
抗瘤能力、安全性得到验证
那么上面一系列的精心设计有没有提高阿得贝利单抗的抗癌活性和安全性呢?
在临床前的IFN-γ释放实验中,研究人员发现阿得贝利单抗刺激T细胞释放IFN-γ的EC50值更低,说明阿得贝利单抗激活T细胞的能力强。
现在回头看CAPSTONE-1研究数据的话,就会发现创纪录的中位OS(阿得贝利单抗+化疗 vs 单纯化疗:15.3个月 vs 12.8个月)[7],也印证了阿得贝利单抗具有很强的抗肿瘤活性。
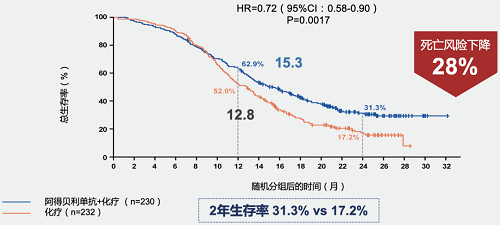
▲ 阿得贝利单抗联合化疗一线治疗mOS达15.3个月,显著优于单纯化疗
阿得贝利单抗的安全性数据也是非常值得关注,CAPSTONE-1研究表明,阿得贝利单抗联合化疗治疗组的≥3级免疫相关不良事件发生率低,均不超过1.8%[7]。从因任何不良事件(AE)导致的死亡和停药率来看,阿得贝利单抗相较其他已经获批ES-SCLC适应证的PD-1/PD-L1抑制剂也更低[3,5,15]。
阿得贝利单抗的正式获批上市,背后凝聚了众多科学家、研究者的智慧和心血。同时也是中国创新药发展的一个缩影,体现着中国自主研发实力的提高。总的来说,阿得贝利单抗的研发从抗体选择到抗体改造,都没有跟随进口PD-L1抑制剂的研发思路,彰显了国产创新药研发的新力量,期待阿得贝利单抗未来能够造福更多中国小细胞肺癌患者。
声明:本文仅供医学药学专业人士作为学术参考,不得用于商业活动。
参考文献:
[1].van Meerbeeck JP, Fennell DA, De Ruysscher DK. Small-cell lung cancer. Lancet. 2011;378(9804):1741-1755. doi:10.1016/S0140-6736(11)60165-7
[2].Network NCC. NCCN clinical practice guidelines in oncology: small cell lung cancer, version.3. https://www.nccn.org/professionals/physician_gls/pdf/nscl.pdf.
[3].Horn L, Mansfield AS, Szczęsna A, et al. First-Line Atezolizumab plus Chemotherapy in Extensive-Stage Small-Cell Lung Cancer. N Engl J Med. 2018;379(23):2220-2229. doi:10.1056/NEJMoa1809064
[4].Liu SV, Reck M, Mansfield AS, et al. Updated Overall Survival and PD-L1 Subgroup Analysis of Patients With Extensive-Stage Small-Cell Lung Cancer Treated With Atezolizumab, Carboplatin, and Etoposide (IMpower133). J Clin Oncol. 2021;39(6):619-630. doi:10.1200/JCO.20.01055
[5].Paz-Ares L, Dvorkin M, Chen Y, et al. Durvalumab plus platinum-etoposide versus platinum-etoposide in first-line treatment of extensive-stage small-cell lung cancer (CASPIAN): a randomised, controlled, open-label, phase 3 trial. Lancet. 2019;394(10212):1929-1939. doi:10.1016/S0140-6736(19)32222-6
[6].Goldman JW, Dvorkin M, Chen Y, et al. Durvalumab, with or without tremelimumab, plus platinum-etoposide versus platinum-etoposide alone in first-line treatment of extensive-stage small-cell lung cancer (CASPIAN): updated results from a randomised, controlled, open-label, phase 3 trial. Lancet Oncol. 2021;22(1):51-65. doi:10.1016/S1470-2045(20)30539-8
[7].Wang J, Zhou C, Yao W, et al. Adebrelimab or placebo plus carboplatin and etoposide as first-line treatment for extensive-stage small-cell lung cancer (CAPSTONE-1): a multicentre, randomised, double-blind, placebo-controlled, phase 3 trial. Lancet Oncol. 2022;23(6):739-747. doi:10.1016/S1470-2045(22)00224-8
[8].Chen Y, Pei Y, Luo J, et al. Looking for the Optimal PD-1/PD-L1 Inhibitor in Cancer Treatment: A Comparison in Basic Structure, Function, and Clinical Practice. Front Immunol. 2020;11:1088. doi:10.3389/fimmu.2020.01088
[9].Vidarsson G, Dekkers G, Rispens T. IgG subclasses and allotypes: from structure to effector functions. Front Immunol. 2014;5:520. doi:10.3389/fimmu.2014.00520
[10].Caaveiro JM, Kiyoshi M, Tsumoto K. Structural analysis of Fc/FcγR complexes: a blueprint for antibody design. Immunol Rev. 2015;268(1):201-221. doi:10.1111/imr.12365
[11].Sun C, Mezzadra R, Schumacher TN. Regulation and Function of the PD-L1 Checkpoint. Immunity. 2018;48(3):434-452. doi:10.1016/j.immuni.2018.03.014
[12].Liu R, Oldham RJ, Teal E, Beers SA, Cragg MS. Fc-Engineering for Modulated Effector Functions-Improving Antibodies for Cancer Treatment. Antibodies (Basel). 2020;9(4):64. doi:10.3390/antib9040064
[13].Bianchini R, Karagiannis SN, Jordakieva G, Jensen-Jarolim E. The Role of IgG4 in the Fine Tuning of Tolerance in IgE-Mediated Allergy and Cancer. Int J Mol Sci. 2020;21(14):5017. doi:10.3390/ijms21145017
[14].Labrijn AF, Buijsse AO, van den Bremer ET, et al. Therapeutic IgG4 antibodies engage in Fab-arm exchange with endogenous human IgG4 in vivo. Nat Biotechnol. 2009;27(8):767-771. doi:10.1038/nbt.1553
[15].Cheng Y, Wang J, Zhou C, et al. Adebrelimab or placebo plus carboplatin and etoposide as first-line treatment for extensive-stage SCLC: A phase 3 trial. Presented at AACR 2022; April 8-13, 2022. Abstract CT038.