2024-06-25
恒瑞创新药SHR-1701研究成果荣登《Cancer Cell》,有望为不可切Ⅲ期非小细胞肺癌患者治疗带来新选择
6月20日,由吴一龙教授团队牵头,恒瑞医药自主研发的PD-L1/TGF-βRII双抗SHR-1701联合或不联合化疗新辅助治疗不可切除的Ⅲ期非小细胞肺癌的概念验证2期临床研究(TRAILBLAZE研究)成果,正式全文在线发表于国际权威学术期刊《Cancer Cell》(影响因子50.3)。TRAILBLAZE研究结果显示1,在接受新辅助联合治疗的主要队列患者(n=97)中,两项主要终点均达到,诱导后的客观缓解率(ORR)为58% (95% CI 47 ~ 68),18个月无事件生存率(EFS)为56.6%(95% CI 45.2 ~ 66.5)。27例(25%)患者接受了手术治疗,均达到R0切除,其中,主要病理缓解(MPR)为44%,完全病理缓解(pCR)为26%;手术治疗组18个月EFS率为74.1% (95% CI 53.2 ~ 86.7),放疗组18个月EFS率为57.3%(43.0 ~ 69.3)。在不可切除的Ⅲ期非小细胞肺癌(NSCLC)患者中,新辅助SHR-1701联合化疗(随后进行手术或放疗)显示出具有前景的疗效和可耐受的安全性。在相当比例的患者(四分之一)中,手术转化是可行的,并且与较好的生存结局相关。

研究背景
基于免疫(IO)的诱导治疗提高了肿瘤/淋巴结降期率、完全切除率和微转移监测率,为无驱动基因突变的可切除NSCLC的有效治疗提供了希望2。放化疗后的巩固治疗是目前不可切除的Ⅲ期NSCLC的标准治疗3,4。我们假设添加新辅助IO可能会进一步改善预后:1. 新辅助IO的手术转化可能是可行的;2. 手术转化有可能转换为长期生存获益。SHR-1701是一种靶向PD-L1和TGF-β的新型双功能融合蛋白5,6。我们开展了一项概念验证试验,在未经治疗的不可切除Ⅲ期NSCLC中评估了新辅助SHR-1701联合或不联合化疗,以及随后的手术或放疗结果。
研究设计
TRAILBLAZER是一项在中国20家医疗中心开展的开放标签、2期试验。患者纳入标准如下:年龄18~70岁,患组织学/细胞学确诊的Ⅲ期NSCLC(根据AJCC第8版),并且MDT(至少一名胸外科医师、一名放射科医师和一名肿瘤内科医师)认为手术不可切除。在这项2期试验(NCT04580498)中,MDT评估为手术不可切除的Ⅲ期NSCLC接受了新辅助SHR-1701联合或不联合化疗,随后接受了手术或放疗治疗,然后SHR-1701巩固治疗。主要研究终点为诱导后ORR和18个月EFS率。A+B组(接受新辅助免疫+化疗的患者)是主要分析队列。
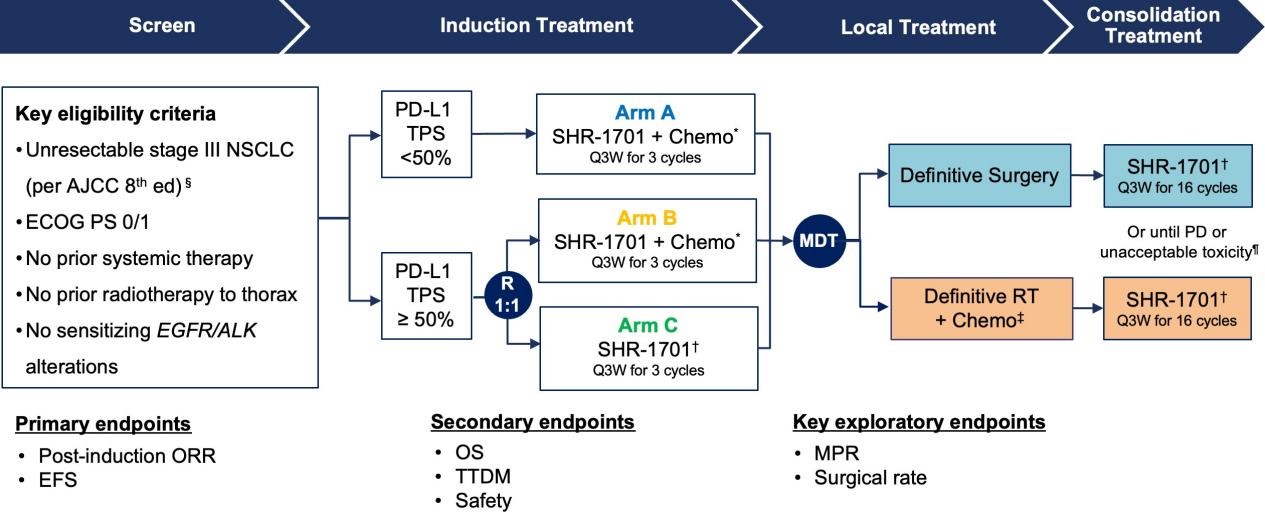
图1 研究设计7
§如果可以采用根治性手术(无需全肺切除即可达到R0切除)和系统性淋巴结清扫,则认为该疾病可切除;不可切除N疾病的推荐标准:认为不可能进行大范围、多站或完全切除。*SHR-1701(30 mg/kg,D1)+紫杉醇(175 mg/m2,D1)+卡铂(AUC 5,D1)。†SHR-1701 (30 mg/kg) 。‡RT (60 Gy/30次)+同步顺铂(30 mg/m2,QW). ¶如果研究者认为有临床益处,则允许在进展后进行治疗。
研究结果
1. 患者基线特征
从2020年11月20日至2022年1月27日,107例患者被分配接受SHR-1701联合化疗的新辅助治疗(A组,88例;B组,n=9)或新辅助SHR-1701单药治疗C组(n=10)(见研究设计图)。A+B组(主要分析队列)达到了计划的样本量,但探索性c组未达到计划的样本量。纳入的所有患者均接受了治疗,并被纳入疗效和安全性分析。大多数患者为男性(94%),当前吸烟者或既往吸烟者(90%),鳞状细胞癌(74%)。大多数患者在基线时表现为ⅢB期(44%)/ⅢC期(30%);18%的患者PD-L1 TPS≥50%。(表1)
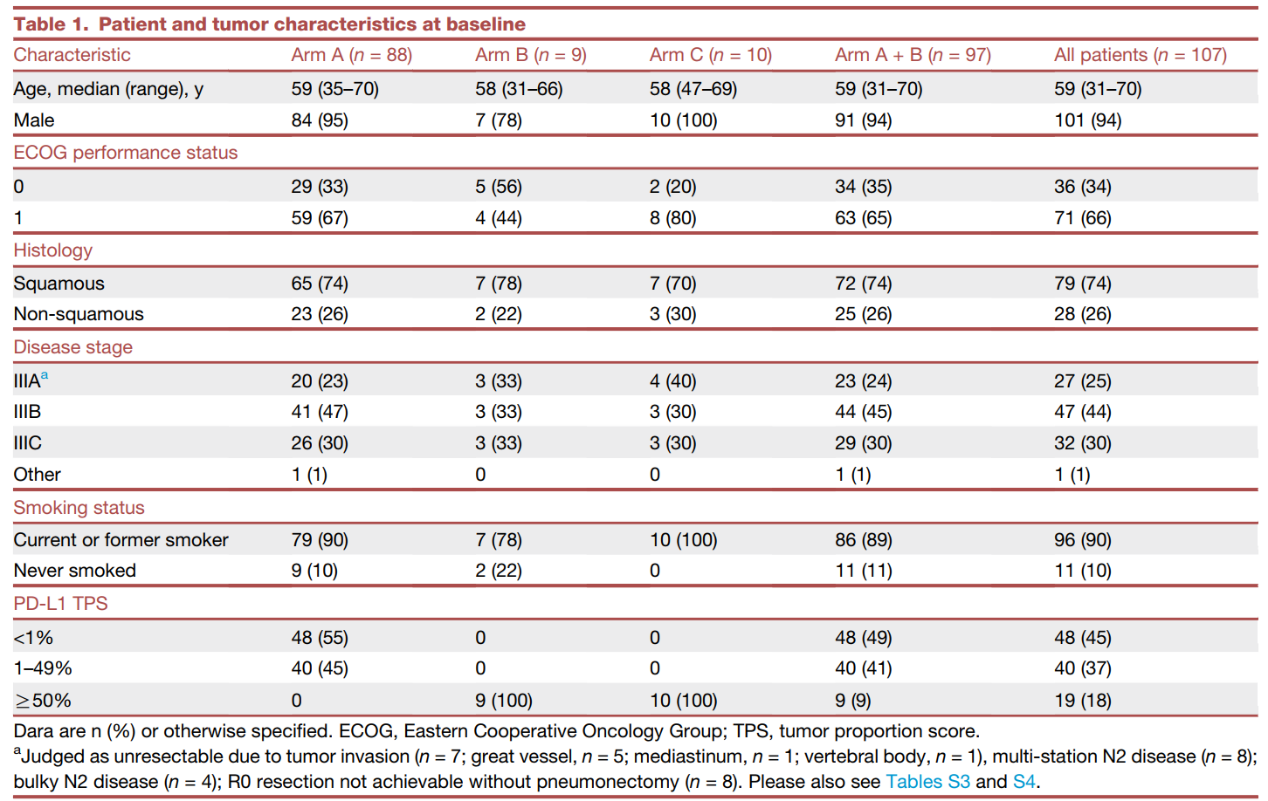
表1 患者基线特征
截至2023年9月30日,中位随访时间为22.2个月。107例患者中,99例(93%)完成诱导治疗,86例(80%)随后接受了局部治疗(手术,n=27;放疗,n=59)。
2. EFS与肿瘤缓解
在主要终点分析中,56例(58%;95% CI 47~68)患者在诱导治疗后达到客观缓解,包括1例(1%)完全缓解和55例(57%)部分缓解(表2)。18个月无事件生存(EFS)率为56.6% (95% CI 45.2~66.5;图2A)。A+B组达到了诱导后ORR和EFS这两项主要终点。C组中,4例(40%;95% CI 12~74)患者达到诱导后缓解(均为部分缓解)(表2);2例(20%)发生EFS事件,18个月EFS率为77.1% (95% CI 34.5~93.9)(图2B)。
在所有治疗组中,诱导治疗后的ORR为56% (95% CI 46~66), 18个月EFS率为58.3% (95% CI 47.4~67.7)(表2,图2C)。诱导后A+B组的疾病控制率(DCR)为93%(95%CI 86~97),C组为90%(95%CI 56~100),所有患者的DCR为93%(95%CI 86~97)(表2)。
数据截止时,A+B组中位EFS为24.2个月(95% CI 12.0~未达到[NR]),C组为未达到;所有患者的中位EFS为24.4个月(95% CI 14.0~NR);12个月EFS率分别为60.5% (95% CI 49.1~70.1)、90.0% (95% CI 47.3 ~ 98.5)和63.0% (95% CI 52.2~72.0)(图2A-C)。A+B组12个月和24个月的总生存率(OS)分别为86.8%(95%CI 77.9~92.3)和78.3%(95%CI 68.0~85.7),所有患者的12个月和24个月OS率分别为87.9%(95%CI 79.6~92.9)和79.9%(95%CI 70.2~86.8)。
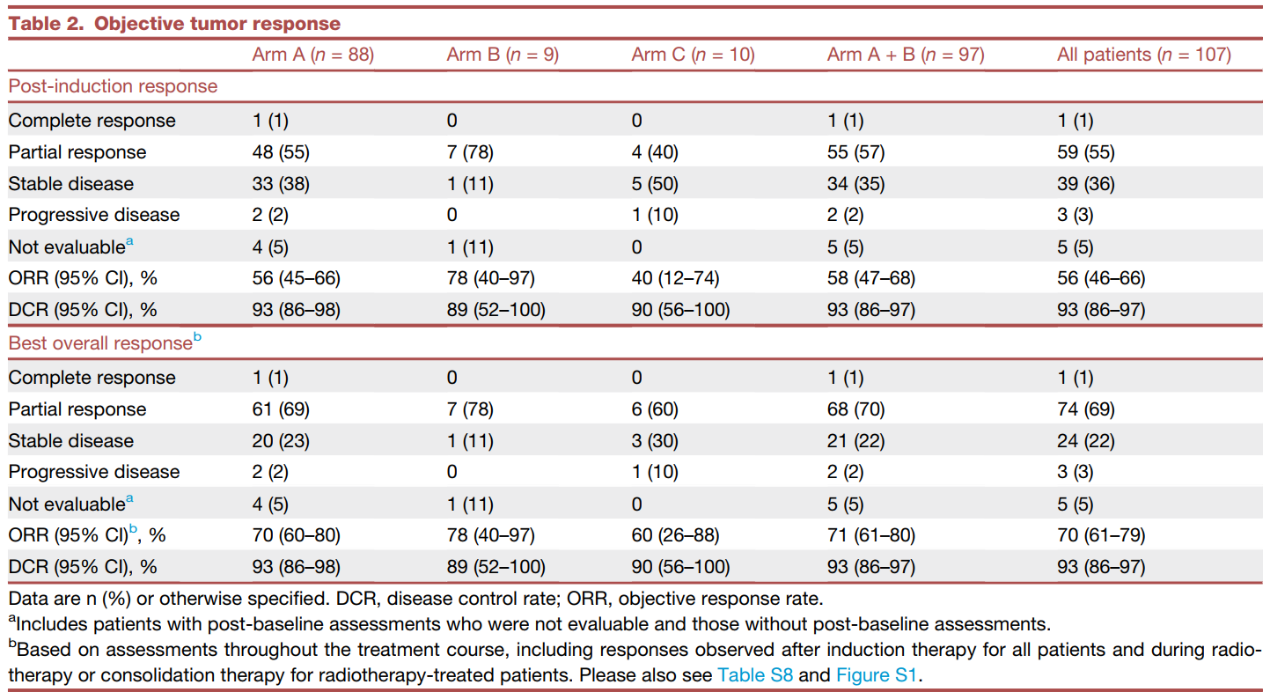
表2 肿瘤客观缓解
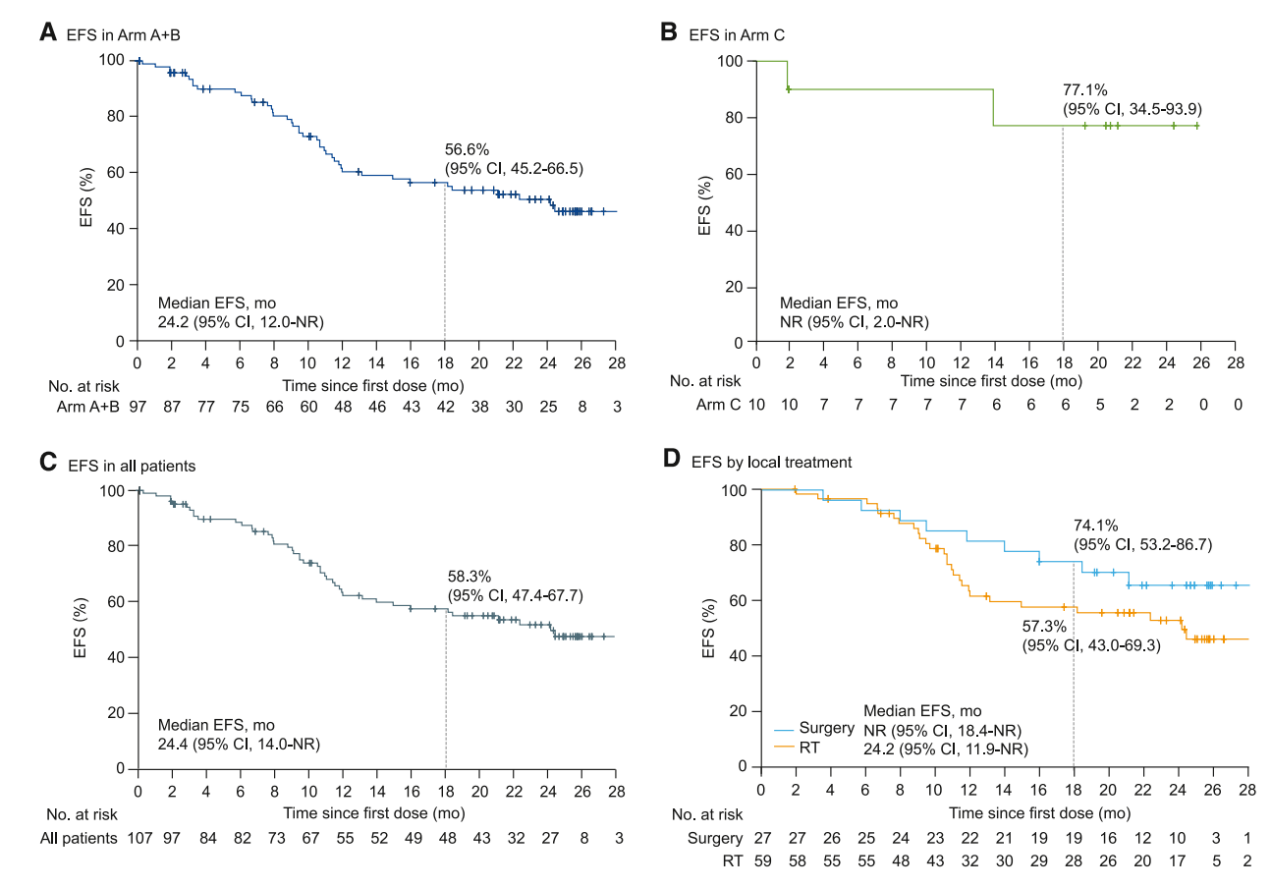
图2 EFS Kaplan-Meier分析
3. 手术结果
107例患者中有27例(25%)接受了手术,A+B组和C组的手术转化率分别25%(24/97)和30%(3/10);基线分期为Ⅲa期、Ⅲb期和Ⅲc期的患者中,手术转化率分别37%(10/27)、26%(94/47)和16%(5/32)。手术切除的27例患者均达到R0切除,12例(44%)为主要病理缓解(MPR)和7例(26%)为完全病理缓解(pCR)(图3)。
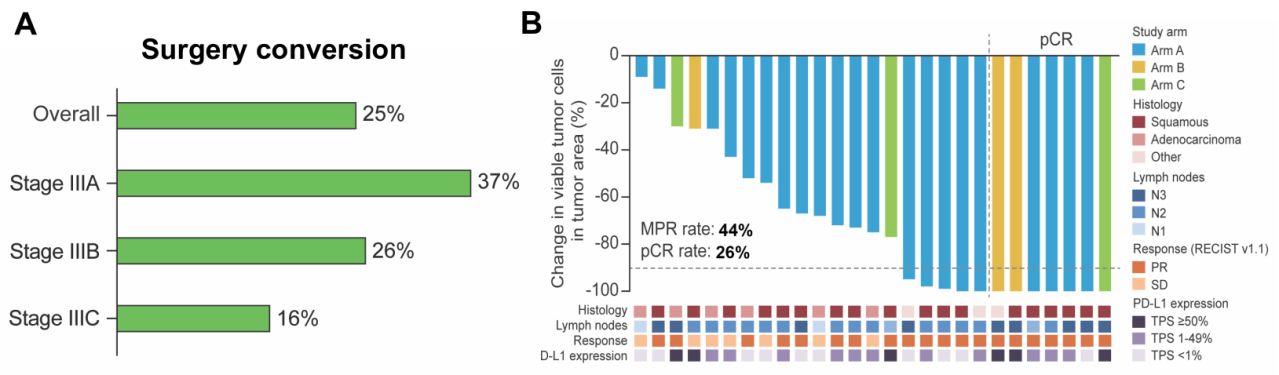
图3 手术转化和病理缓解结果
手术切除患者中位EFS未达到(95% CI 18.4~NR),放疗患者中位EFS为24.2个月(95% CI 11.9~NR);12个月EFS率分别为81.5%(95% CI 61.1~91.8)和61.3%(95% CI 46.9~72.8),18个月EFS率分别为74.1%(95% CI 53.2~86.7)和57.3%(95% CI 43.0~69.3)(图2D)。
4. 安全性
安全性结果显示,没有出现新的安全信号,总体不良反应安全可耐受。
研究结论
在不可切除的Ⅲ期NSCLC中,新辅助SHR-1701联合化疗(随后进行手术或放疗)显示出有前景的抗肿瘤活性,并且安全性可耐受。研究证实1/4的患者实现了手术转化,并转化为较好的生存结局。
参考文献:
1. Qing Zhou, et al. Neoadjuvant SHR-1701 with or without chemotherapy in unresectable stage III non-small-cell lung cancer: A proof-of-concept, phase 2 trial. Cancer Cell. Published:June 20, 2024. DOI:https://doi.org/10.1016/j.ccell.2024.05.024.
2. Mountzios Giannis, et al. Immune-checkpoint inhibition for resectable non-small-cell lung cancer - opportunities and challenges. Nat Rev Clin Oncol.. 20,10 (2023): 664-677. doi:10.1038/s41571-023-00794-7
3. Antonia Scott J, et al. Durvalumab after Chemoradiotherapy in StageⅢ Non-Small-Cell Lung Cancer. N Engl J Med. 377,20 (2017): 1919-1929.
doi:10.1056/NEJMoa1709937
4. Qing Zhou, et al. Sugemalimab versus placebo after concurrent or sequential chemoradiotherapy in patients with locally advanced, unresectable, stageⅢ non-small-cell lung cancer in China (GEMSTONE-301): interim results of a randomised, double-blind, multicentre, phase 3 trial. Lancet. Oncol. 23,2 (2022): 209-219. doi:10.1016/S1470-2045(21)00630-6
5. Dan Liu, et al. Bifunctional anti-PD-L1/TGF-βRII agent SHR-1701 in advanced solid tumors: a dose-escalation, dose-expansion, and clinical-expansion phase 1 trial. BMC Med. 20,1(2022): 408. doi:10.1186/s12916-022-02605-9
6. Ji-Feng Feng, et al. SHR-1701, a Bifunctional Fusion Protein Targeting PD-L1 and TGFβ, for Recurrent or Metastatic Cervical Cancer: A Clinical Expansion Cohort of a Phase I Study. Clin Cancer Res. 28,24 (2022): 5297-5305.
doi:10.1158/1078-0432.CCR-22-0346
7. Yi-Long Wu, et al. J Clin Oncol 42, 2024 (suppl 16; abstr 8082) . doi:10.1200/JCO.2024.42.16_suppl.8082
声明:
1. 本新闻旨在分享研发前沿资讯,仅供医疗卫生专业人士基于学术目的参阅,非广告用途。
2. 恒瑞医药不推荐任何未被批准的药品、适应症的使用。